なんでだろう?
回路につないだ食塩を炎であぶると、LEDが点灯して通電を示しました。
そうなんだ!
食塩水が電気を通すことはよく知られています。それでは、固体の食塩や、高温に熱して溶かした液体の食塩は電気を通すのでしょうか。食塩が溶けて液体になる温度(融点)は約800℃で、とても高いのですが、ごく少量の食塩をガスの炎で直接あぶると、家庭でも簡単に溶かすことができるので、実際に確かめてみましょう。
食塩を電極の間にはさみ、電流が流れるとLEDが点灯する回路を作ります。食塩が固体のときはLEDは消えていますが、加熱すると徐々に明るく点灯し、炎を消すとLEDも消えます。食塩が高温に加熱され、液体になっている間だけ電流が流れるのです。
食塩の主成分の塩化ナトリウムは、プラスの電気を帯びた陽イオンとマイナスの電気を帯びた陰イオンの結晶です。固体のときはイオン同士がしっかり結合していますが、水に溶かすとイオンがばらばらになります。食塩水に電圧をかけると、イオンが移動することで電流が流れます。一方、塩化ナトリウムを約800℃まで加熱すると、イオンの結合が解けて動きやすくなります。そのため、やや高い電圧をかけると、液体の塩化ナトリウムでも電流が流れるのです。
①太めの縫い針 2本
②割りばし 1本
③かなづち
④赤色LED 1個
⑤9V乾電池 1個
⑥クリップ付きリード線 3本
⑦ブックエンド 1個
⑧目玉クリップ 1個
⑨アルミホイル
⑩食塩
⑪着火用ガスライター
・セロハンテープ

実験で使用した材料の詳細
・太めの縫い針 DAISO 手芸針No.4(ふとん針2本φ1.06×70mmを使用)
・割りばし 元林 割り箸 50膳 裸
・かなづち DAISO パイプハンマー
・赤色LED 秋月電子通商 超高輝度5mm広角赤色LED OS5RKA5B61P
・9V乾電池 DAISO GP SUPERマンガン乾電池9V形 6F22(PU)
・ブックエンド DAISO ブックエンド 13.5cm×20cm×10cm No.62
・目玉クリップ サンケーキコム 目玉クリップ 小 MD-3A
・アルミホイル DAISO アルミホイル
・食塩 ローソン 瀬戸内の塩(しっとりタイプ)
・ガス式着火ライター 東海 CRチャッカマン
※実験材料の一例です。準備する際の参考にしてください。
![]()
[実験の注意]
・NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものであり、工作の完成品は市販品と同等、もしくは代用品となるものではないことを理解したうえで、個人の責任において実験を行ってください。
・必ず手順を読んでから工作・実験を行ってください。
・器具の取り扱いには十分注意し、けがをしないようにしましょう。
・小学生など低年齢の方が実験を行う場合は、必ず保護者と一緒に行ってください。
-
1
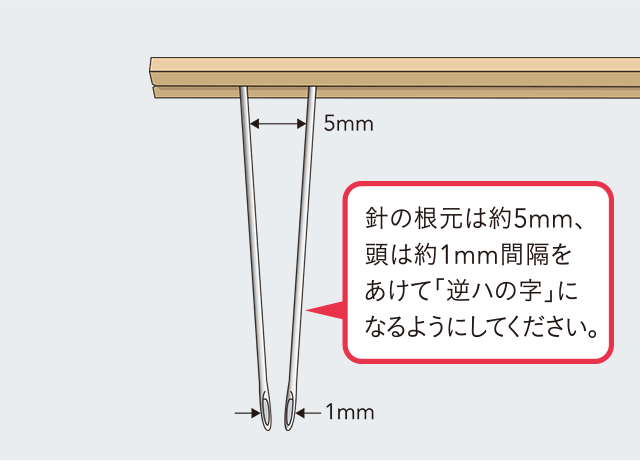
2本の針を図のように割りばしにかなづちで軽く打ち込みます。
-
2
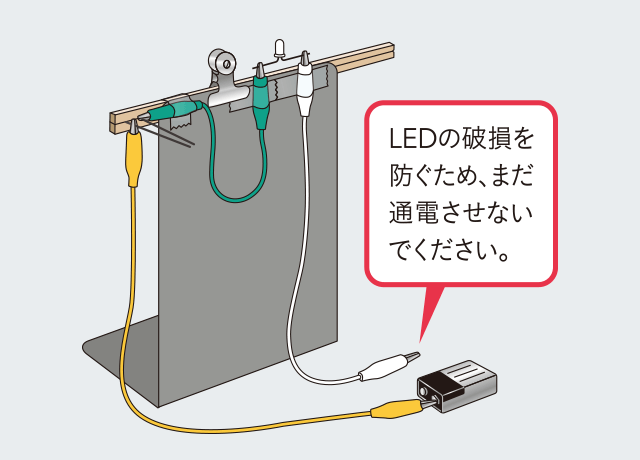
ブックエンドに割りばしをクリップでとめ、針、乾電池、LEDをリード線で図のようにつなぎます。
-
3

溶けた食塩は非常に高温になるので、装置の下にアルミホイルを敷きます。針の頭に食塩をのせ、乾電池を接続します。
※ライターの炎の近くに可燃物を置かないなど、安全に十分注意してください。 -
4
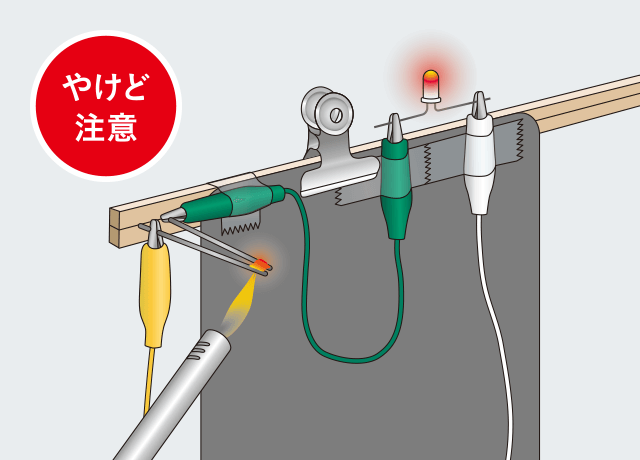
ガスライターの炎で斜め下から食塩をあぶり、LEDを観察します。
※針や塩は高温なため、冷めるまで直接触らないでください。
※ライターの使用上の注意に従い、長時間加熱し続けないでください。LEDが点灯したら、速やかに火を消してください。
実験を成功させるコツとヒント
・塩はサラサラに加工されたものや味のついたものは使わず、普通の食塩を使ってください。
・ガスライターは、必ずノズルの長い着火用を使ってください。
・ライターの炎は中心部より先端部の方が高温なので、炎の先端であぶってください。
溶けた熱い塩が意外なところで大活躍
固体の塩を加熱して溶かし、液体にしたものを溶融塩(ようゆうえん)または融解塩(ゆうかいえん)といいます。塩を水に溶かした食塩水などと違ってあまりなじみがありませんが、工業の分野では非常に重要な役割を果たしています。実験でもわかるように、溶融塩は電気を通しやすいという特徴があります。さらに、さまざまな物質をよく溶かし、高温でも化学的に安定しているなどの性質から、アルミニウムやマグネシウムといった金属の精練やフッ素などの化学物質の製造、金属の表面加工に利用されてきました。近年では、太陽熱発電の蓄熱材として再生可能エネルギーの普及にも貢献しています。さらに、未来のエネルギー源として期待される燃料電池の材料としても注目される素材です。
電気の強い絆で結びついたイオン結晶
イオンはプラスの電気を帯びた陽イオンと、マイナスの電気を帯びた陰イオンからなり、陽イオンと陰イオンは引き合ってくっつきます(イオン結合)。陽イオンと陰イオンが規則正しく並び、イオン結合でしっかりくっついたものをイオン結晶といいます。食塩(塩化ナトリウム)の粒を虫めがねで拡大すると、サイコロのような正六面体の結晶構造が見られます。炭酸カルシウムの結晶である大理石や、酸化アルミニウムの結晶であるルビーやサファイアも、イオン結晶の代表です。イオン結晶は非常に強力な力で結びついているので硬く、溶けにくく、常温では電気を通さないという共通の特徴があります。しかし、高温に熱して液体になると、イオンが自由に移動して電流が流れるのです。
一方、ガラスも溶けると電流が流れるのですが、食塩とはその様子が少し異なります。一般的なガラスは、主成分であるケイ素と酸素の原子が不規則につながり、そこにイオンが混じった構造なので、加熱すると原子の結合がゆるんでイオンが動けるようになります。しかし、イオン結晶ではないので電流は弱く、壊れやすいという性質があります。
NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものです。工作の完成品は市販品と同等ではなく、代用品にもならないことを理解したうえで、個人の責任において実験を行ってください。
NGKサイエンスサイトは日本ガイシが運営しています。ご利用に当たっては、日本ガイシの「プライバシーポリシー」と「ご利用条件•ご注意」をご覧ください。
本サイトのコンテンツ利用に関しては、本サイトお問い合わせ先までご相談ください。





