なんでだろう?
シャボン玉が水面に近づくと、何かに乗ったように、ほぼ同じ高さで動きが止まります。
そうなんだ!
空中に放たれたシャボン玉は、ふわふわとただよいながらも重力に引っぱられて少しずつ落下していきます。ところがこのシャボン玉は、水の入った容器の上で落下を止め、しばらくの間、ほぼ同じ高さで静止しています。いったいどんな仕掛けなのでしょう?
実は、容器の水に重曹とクエン酸を溶かしておいたのです。
重曹は炭酸水素ナトリウムという物質です。クエン酸などの酸性の溶液と反応して二酸化炭素を発生させます。二酸化炭素は空気よりも重いので、水面近くにたまります。中に空気が入ったシャボン玉が落下してくると、二酸化炭素の中では浮力を得て浮かび、浮力と重力のバランスがとれる一定の高さで高さで静止します。
①ボウルや水槽などの容器
②重曹
③クエン酸
④計量スプーン大さじ
⑤計量カップ
⑥市販のシャボン液
⑦シャボン液に付属の吹き具
・水
※シャボン液は、台所用中性洗剤を5倍にうすめたもので、吹き具は、ストローの先に約2mm間隔で縦に約5mm切り込みを入れたもので代用できます。

実験で使用した材料の詳細
・ボウル 大創産業 ステンレスボウル(内径:24cm)
・重曹 大創産業 落ち落ちV 重曹350g
・クエン酸 大創産業 落ち落ちV クエン酸200g
・計量スプーン エコー金属 計量スプーン3本組
・計量カップ 大創産業 計量カップ(容量250ml)
・シャボン液/吹き具 大創産業 シャボン玉セット 4コ入(吹き具付き)、
しゃぼん玉 吹き棒12本入(シャボン玉液1本/吹き棒12本)
![]()
[実験の注意]
・NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものであり、工作の完成品は市販品と同等、もしくは代用品となるものではないことを理解したうえで、個人の責任において実験を行ってください。
・必ず手順を読んでから工作・実験を行ってください。
・器具の取り扱いには十分注意し、けがをしないようにしましょう。
・小学生など低年齢の方が実験を行う場合は、必ず保護者と一緒に行ってください。
・重曹とクエン酸を多量に反応させたり、容器内に顔を突っ込んだりしないで下さい。発生した二酸化炭素により、酸素欠乏症を引き起こす恐れがあります。
-
1

重曹とクエン酸を計量スプーン大さじ2杯ずつ容器に入れ、水300mLを注いで軽くかき混ぜます。
-
2
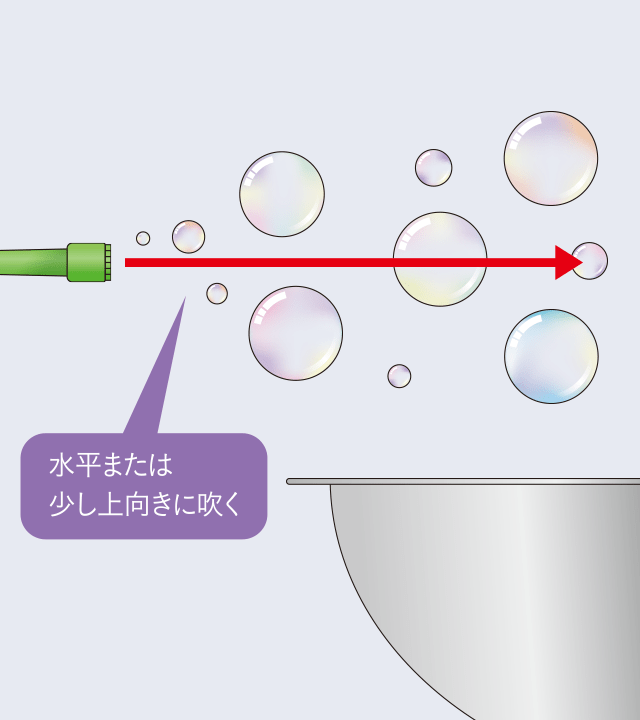
反応による泡立ちが落ち着いたら、付属の吹き具にシャボン液をつけて吹き、容器の上にシャボン玉を飛ばします。
※シャボン液を吸い込まないようにしてください。 -
3
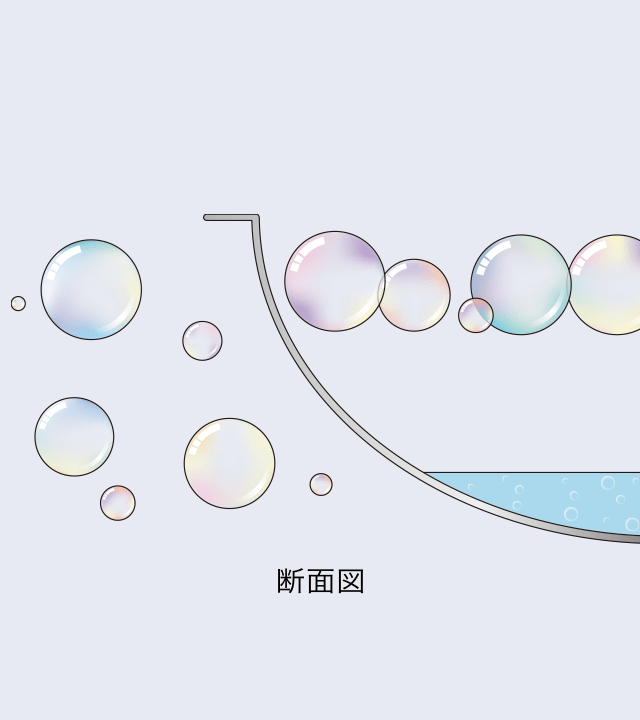
容器の中のシャボン玉と、容器の外のシャボン玉の動きを観察します。
※二酸化炭素の濃度が薄くなったら、重曹を大さじ1杯加えてください。
実験を成功させるコツとヒント
・二酸化炭素が激しく発生していると、水滴が飛んでシャボン玉が割れやすくなります。反応が落ち着いて泡立ちが少なくなってからシャボン玉を吹いてください。
・大きなシャボン玉より、中小のシャボン玉を数多く飛ばした方が成功しやすくなります。
発生させた気体を使って二酸化炭素の性質を調べよう
二酸化炭素は物を燃やしたときや、生物の呼吸によって発生する身近な気体です。空気中にもごくわずかですが、0.03%ほど含まれます。二酸化炭素には、実験でわかるように空気より重い(約1.5倍)ということのほかに、水素のように自らが燃えることもなく、酸素のように他の物が燃えるのを助けることもないという特徴があります。短く切ったロウソクを針金を曲げたものに取り付け、火をつけて実験で使った容器の中に入れてみましょう。すぐに火が消えるので、発生している気体が二酸化炭素であることがわかります。二酸化炭素のこの特徴は、消火器などに利用されて役立っています。
いろいろあります。二酸化炭素の作り方
二酸化炭素は炭素原子1個と酸素原子2個がくっついた化合物です。炭素も酸素も地球上ではありふれた物質であり、二酸化炭素を使った製品は身の回りでも多く使われているので、いろいろな方法で二酸化炭素を生成することができます。
炭酸飲料の泡や発泡入浴剤の泡は二酸化炭素なので、それらから集めることが可能です。発泡入浴剤には重曹とクエン酸が使われており、今回の実験と同じしくみで二酸化炭素が発生します。ドライアイスを使う方法もあります。ドライアイスは二酸化炭素を冷やして固体にしたものです。溶けると、液体を経ずに気体の二酸化炭素に戻ります(昇華)。
学校の理科の授業では、石灰石や貝がらなどにうすい塩酸をかける方法が一般的です。石灰石や貝がらの主な成分は炭酸カルシウムという物質です。炭酸カルシウムは炭素と酸素を含んでおり、塩酸によって分解されて二酸化炭素が発生します。工業的には、石炭を加熱する工程や、石油を精製する工程などで排出される二酸化炭素を利用し、大量に生産しています。
NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものです。工作の完成品は市販品と同等ではなく、代用品にもならないことを理解したうえで、個人の責任において実験を行ってください。
NGKサイエンスサイトはNGKが運営しています。ご利用に当たっては、NGKの「プライバシーポリシー」と「ご利用条件•ご注意」をご覧ください。
本サイトのコンテンツ利用に関しては、本サイトお問い合わせ先までご相談ください。





