なんでだろう?
水道水、食塩水、金属で電流の流れ方が違うのはなぜ?
そうなんだ!
LEDの明るさで電流の強さがわかる電流チェッカー(簡易電流計)を作りました。
この装置で水道水、食塩水、金属を調べると、食塩水は水道水より電流がよく流れ、金属より流れにくいことがわかります。この違いはなぜ起こるのでしょう?
金属に電流がよく流れるのは、金属中の自由電子のはたらきです。金属に電圧をかけると、マイナスの電気を帯びた電子はプラス極側に引っぱられます。これが、金属を流れる電流の正体です。
次に、食塩水はどうでしょう。食塩(塩化ナトリウム)を水に溶かすと、プラスの電気を帯びた陽イオンと、マイナスの電気を帯びた陰イオンに分かれます。食塩水に電圧をかけると、陽イオンはマイナス極へ、陰イオンはプラス極へ引っぱられます。これが、食塩水に流れる電流です。イオンは電子よりけた違いに大きくて移動しにくいので、金属と比べると電流が流れにくくなります。
また、純粋な水はほとんど電気を通しませんが、水道水には微量のイオンが含まれるので、わずかに電流が流れます。
1. 赤色LED(透明カバーの高輝度タイプ)1個
2. 3Vコイン型電池 1個
3. ゼムクリップ 1個
4. 金属製のフォークやナイフ、スプーンなど
5. 食塩
6. 小皿 2枚
・コップ
・水道水
・かきまぜるスプーンなど

実験で使用した材料の詳細
・LED LED PARADISEエルパラ 超高輝度5mm赤色LED
・コイン電池 三菱 リチウム電池 CR2016
・ゼムクリップ アスクル ゼムクリップ小(28mm)
・金属のフォーク ニトリ ヒメフォーク
・食塩 ジャパンソルト 塩1kg
・小皿 大創産業 ニューボーン丸皿 約10cm
![]()
[実験の注意]
・NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものであり、工作の完成品は市販品と同等、もしくは代用品となるものではないことを理解したうえで、個人の責任において実験を行ってください。
・必ず手順を読んでから工作・実験を行ってください。
・器具の取り扱いには十分注意し、けがをしないようにしましょう。
・小学生など低年齢の方が実験を行う場合は、必ず保護者と一緒に行ってください。
-
1
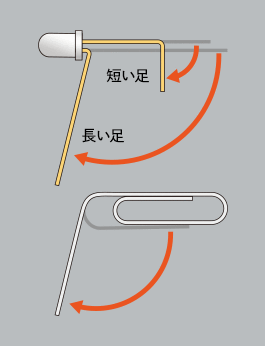
LEDの足とゼムクリップを図のように曲げます。
-
2
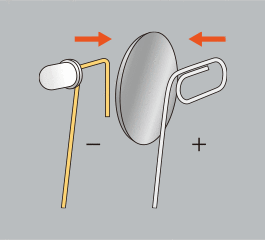
コイン電池のマイナス極にLEDの短い足を、プラス極にゼムクリップを押し当て、セロハンテープで固定します。
※伸ばしたゼムクリップの先とLEDの長い足の先をそろえてください。 -
3
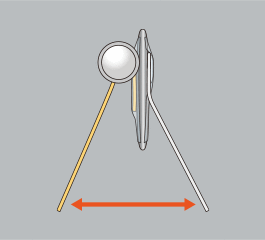
LEDとゼムクリップの足を少し開き、自立できるように調節します。
-
4
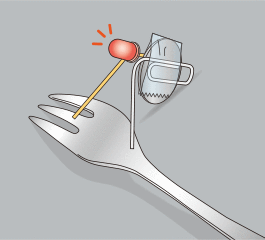
2本の足を金属に当て、LEDが明るく点灯すれば電流チェッカーの完成です。
※測定したいものに2本の足を当て、LEDが光れば電流が流れています。 -
5
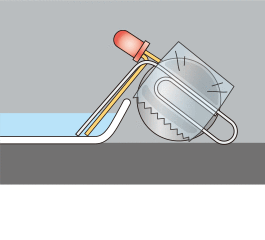
コップに水を入れて食塩を少しずつ溶かし、できるだけ濃い(飽和水溶液に近い)食塩水をつくります。食塩水と水道水を小皿に入れて電流チェッカーで測定し、明るさを比べます。
実験を成功させるコツとヒント
・LEDは超高輝度タイプを使ってください。輝度の低いLEDは、水道水では点灯しない場合があります。
・精製水などの純粋な水は使わないでください。電気をほとんど通さないのでLEDが点灯しません。
原子が電子をやりとりしできるイオン
食塩の主成分である塩化ナトリウムは、ナトリウムと塩素でできています。
しかし、塩化ナトリウムはナトリウム原子と塩素原子が結びついた分子ではありません。プラスの電気を帯びたナトリウムイオンと、マイナスの電気を帯びた塩素イオンが、静電気的な力で結合した結晶なのです。
もともとナトリウム原子は11個の電子を、塩素原子は17個の電子を持っています。ところが、ナトリウム原子は電子を1つ放出しやすく、塩素原子は電子を1つ獲得しやすいという性質があります。
そのため、ナトリウム原子は塩素原子に電子を1つ渡すことでお互いに安定し、イオンの状態でしっかりとした結晶をつくるのです。

電池はイオンのはたらきで電気をつくっている
イオンのはたらきを利用した身近な製品の代表は電池です。電池は、マイナス極の金属の原子が化学反応によって電子を放出して陽イオンに変わり、その電子がプラス極に移動することで電流を生み出します。マンガン電池やアルカリ電池などの乾電池は、化学反応が止まって電子の流れが起きなくなったら使えなくなります。
それでは、スマートフォンやデジタルカメラなどに使われるバッテリー(蓄電池)が、充電するとまた使えるようになるのはなぜでしょう? バッテリーは外部から電圧をかけることで、電子をプラス極からマイナス極へ移動させることができます。するとマイナス極の陽イオンが電子を受け取って金属原子に戻るので、再び電池として使えるのです。
NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものです。工作の完成品は市販品と同等ではなく、代用品にもならないことを理解したうえで、個人の責任において実験を行ってください。
NGKサイエンスサイトはNGKが運営しています。ご利用に当たっては、NGKの「プライバシーポリシー」と「ご利用条件•ご注意」をご覧ください。
本サイトのコンテンツ利用に関しては、本サイトお問い合わせ先までご相談ください。





