どうしてなのかな
あたためた金属を冷水に入れると、金属の熱が冷水に伝わって水の温度は上がります。このとき、金属から出た熱と、水に入った熱の量は同じで、やがて金属と水は同じ温度になります。
種類の異なる同じ重さの金属を100℃にあたため、それぞれを同じ量の0℃の冷水に入れてしばらくすると、どういうわけか水温に差ができます(実験A)。アルミ、鉄、銅の3種類でくらべたら、アルミを入れた水の温度がいちばん高くなりました。同じ重さで同じ温度にしていたのに、どうしてでしょう?
そうかなるほど
重さや大きさなどの条件を一定にした物質の温度を1K(ケルビン※1)上げるのに必要な熱量(単位:J(ジュール))のことを「比熱容量」といいます。重さを一定にしたときの金属の比熱容量は金属の種類によって違い、アルミの比熱容量は鉄や銅にくらべて大きいのです。
同じ重さといっても、アルミと鉄では見た目の大きさがずいぶん違いますね。重さではなく原子の数(モル※2)を一定にしてみるとどうでしょう(実験B)。3種類の金属の大きさがほぼ同じになり、あたためられた水温もほとんど差がありません。つまり、原子の数を一定にしたときの比熱容量は、金属の種類に関係なくほぼ同じといえそうです。実は、多くの固体は1モルあたりの比熱容量がほぼ同じであるという法則(デュロン・プティの法則)があるのです。
軽いアルミは、鉄や銅と同じ重さにすると見た目が大きく、原子の数は多くなります。原子の数が多いから、実験Aではアルミを入れた水がいちばん高い温度になったわけです。
※1:ケルビン(K)
温度をあらわす国際的な基本単位。ふだん、私たちが使っている摂氏(℃)はケルビンで定義されています。例えば0℃は273.15K、100℃は373.15K、その差はともに100。「1K上げる」は「1℃上げる」ことになります。
※2:モル(mol)
物質の量を原子や分子の個数で表現するときに用いる基本単位。原子は非常に小さいので、6.02×1023個をひとまとめにした量が1モルと定められています(12個をひとまとめにして1ダースと呼ぶのと似ています)。1モルの重さは、原子量(原子の質量)にグラム(g)をつけたものと等しくなります。
材料
1. アルミ針金(1.6mm径) 約8.5m
2. 鉄針金(1.6mm径) 約4.5m
3. 銅針金(1.6mm径) 約4m
4. 断熱紙コップ(約250m) 3個


工作の完成品
道具
•はかり(キッチンスケール)
※1g単位で計量できるもの
•軍手
•ニッパー
•菜ばし
•温度計
同じ重さでくらべてみよう
![]()
[実験の注意]
・NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものであり、工作の完成品は市販品と同等、もしくは代用品となるものではないことを理解したうえで、個人の責任において実験を行ってください。
・工作・実験を行う際は、必ず手順を読んでから行ってください。
・器具の取り扱いには十分注意し、けがをしないようにしましょう。
・小学生など低年齢の方が実験を行う場合は、必ず保護者と一緒に行ってください。
-
1
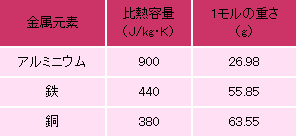
(1)針金の重さをはかりながら、3種類とも30gになるようにニッパーで切ります。
※安全のために軍手をはめましょう。
(2)サインペンなどに針金を巻いて、紙コップに入る大きさにします。
(100gの水を入れたときに針金が完全にひたるようにしましょう) -
2
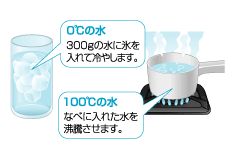
0℃と100℃の水をつくります。
-
3

(1)沸騰している湯に1種類の針金を入れて、1分間あたためます。
(2)0℃に冷やした水を100gだけ紙コップに入れておきます。 -
4

あたためた針金を湯から出してすぐ、紙コップの冷水にひたします。1分たったら菜ばしでかきまぜ、温度計が針金にふれないように注意して水温をはかります。残りの2種類の針金を使って(3)(4)の手順を繰り返し、3種類の水温をくらべます。アルミを入れた水の温度が一番高く、鉄と銅ではあまり差がないことがわかります。
同じ原子数(モル)でくらべてみよう
![]()
[実験の注意]
・NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものであり、工作の完成品は市販品と同等、もしくは代用品となるものではないことを理解したうえで、個人の責任において実験を行ってください。
・工作・実験を行う際は、必ず手順を読んでから行ってください。
・器具の取り扱いには十分注意し、けがをしないようにしましょう。
・小学生など低年齢の方が実験を行う場合は、必ず保護者と一緒に行ってください。
-
1

3種類の針金それぞれを約0.5モル(アルミ:14g、鉄:28g、銅:32g)の量になるように切り、実験Aの手順(1)と同じように巻きます。
-
2

実験Aの手順(2)~(4)と同じようにして、3種類の水温をくらべます。ほとんど同じ温度になることがわかります。
NGKサイエンスサイトで紹介する実験は、あくまでも家庭で手軽にできる科学実験を目的としたものです。工作の完成品は市販品と同等ではなく、代用品にもならないことを理解したうえで、個人の責任において実験を行ってください。
NGKサイエンスサイトはNGKが運営しています。ご利用に当たっては、NGKの「プライバシーポリシー」と「ご利用条件•ご注意」をご覧ください。
本サイトのコンテンツ利用に関しては、本サイトお問い合わせ先までご相談ください。





